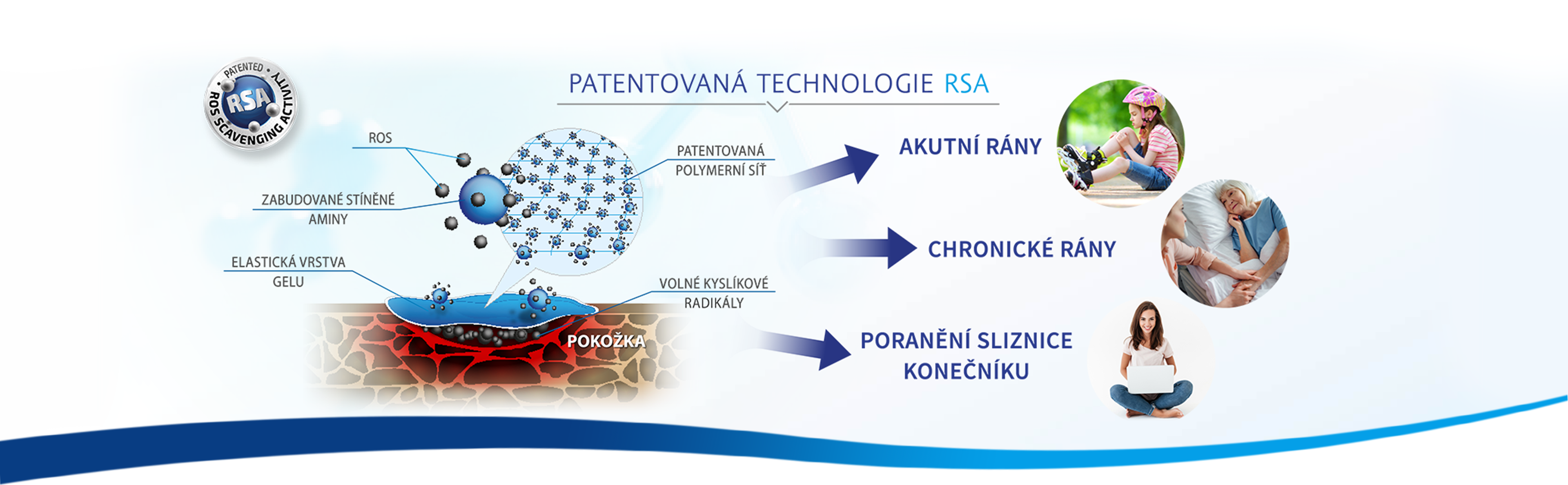
Jedná se o velmi reaktivní částice s nepárovým elektronem, které díky své nestabilitě dokáží narušovat a ničit zdravé buňky a tím zpomalit, nebo dokonce zastavit hojení rány. Hojení narušují volné kyslíkové radikály, které se tvoří všude tam, kde dojde k poranění. V poškozených buňkách jsou často aktivovány enzymy, které samy vytváří tyto radikály a peroxid vodíku, což vede k tomu, že v poškozené tkáni přibývá reaktivních produktů kyslíku. Nadměrná koncentrace ROS způsobuje poškození i zdravých buněk, což vede k rozvoji zánětlivé reakce a zpomaluje tvorbu nové tkáně a tím i hojení rány. Nepříznivý vliv nadměrné produkce ROS na průběh hojení poškozené tkáně je v lékařské literatuře dokumentován již od počátku 90. let minulého století, stejně tak, jako pozitivní vliv látek omezujících působení ROS (např. antioxidanty). Tento bludný kruh lze přetnout jedině vychytáním volných radikálů a tím urychlit celkovou dobu hojení rány, což jde ruku v ruce s finanční úsporou, ale samozřejmě i pohodlím pacienta.


Naše přípravky obsahují patentované polymery různých typů, které ale mají každý do své struktury zabudované stericky stíněné aminy. Tím, mimo jiné , funguje jako velmi účinný lapač reaktivních produktů kyslíku (ROS), které následně převádí na stabilní, pro organismus a zejména pro prostředí nad ranou, neškodné sloučeniny.


Zásadní rozdíl oproti ostatním dostupným přípravkům je, že ÚČINKY NAŠICH PŘÍPRAVKŮ NEZÁVISÍ NA MNOŽSTVÍ VSTŘEBANÉ ÚČINNÉ LÁTKY. Hojivý účinek přípravků a v nich obsažených polymerů je zapříčiněn výhradně jejich chemickou strukturou, která ihned po aplikaci nastolí v ráně IDEÁLNÍ PODMÍNKY a to tím, že eliminují negativní působení ROS a případně mikrobiálního osídlení v ráně.
Charakteristické pro všechny přípravky je , že se nevstřebávají, působí pouze na povrchu rány a jejich účinek se tedy v čase nesnižuje.
Podporují tvorbu granulační tkáně, ale potlačují hypergranulaci. V epitelizační fázi podporují dělení buněk a jejich přerůstání od okrajů rány. Změkčují a zvláčňují novou tkáň, zabraňují kompresi jizvené tkáně a tím stažení okolní pokožky. Ani při dlouhodobém použití nemacerují tkáň.
Přípravek k podpoře hojení zánětlivých onemocnění, který dnes označujeme obchodním názvem HemaGel®, byl vyvinut v Ústavu makromolekulární chemie Akademie věd ČR, v. v. i. Toto špičkové vědecké středisko se vědě a výzkumu věnuje již půl století a dalo vzniknout i jednomu z nejslavnějších českých vynálezů všech dob – kontaktním čočkám.


Historie Ústavu makromolekulární chemie se začala psát v padesátých letech 20. století. Úspěšné vědecké sympozium o makromolekulách, které se konalo v Praze roku 1957, bylo impulsem ke vzniku specializovaného pracoviště zaměřujícího se na toto rychle se rozvíjející vědní odvětví. ÚMCH byl založen v roce 1959 coby součást Akademie věd a jeho prvním ředitelem byl profesor Otto Wichterle, jehož jméno je již navždy spojeno s vynálezem a následně i zahájením výroby měkkých kontaktních a intraokulárních čoček. V posledních letech se ÚMCH zaměřuje na trojici hlavních oblastí: výzkum biomakromolekulárních systémů, zkoumání dynamiky a samoorganizace molekulárních a nadmolekulárních polymerních útvarů a problematika přípravy, charakterizace a využití nových polymerů s řízenou strukturou a vlastnostmi.
V ÚMCH byl od počátku založení kladen důraz rovnoměrně jak na polymerní chemii, tak na polymerní fyziku. Zároveň zde bylo zachováváno hledisko rovnováhy mezi teoretickým, základním a aplikovaným výzkumem. Snaha byla věnována také uplatnění výsledků výzkumu v průmyslové výrobě. Mezi nejvýznamnější praktické výsledky v 60. letech patřila alkalická polymerizace kaprolaktamu a příprava hydrofilních polymerů založených na poly(2-hydroxyethyl methakrylátu).




Výhradní distributor pro ČR a SK.
Targa team a. s. – www.targateam.cz
IČ: 28089529
Firma zapsaná v obchodním rejstříku, spisová značka: B 17224 vedená u Městského soudu v Praze.
Výrobce:
VH Pharma, a. s.
Jakubská 647/2
110 01 Praha 1
www.vhpharma.cz